タンパク質のリボン構造図、格好良くて好きです。コレは、アセチルコリンエステラーゼという酵素の立体構造で、今日はこいつの機能を確認します。
最近僕の中で熱い分子・カルバミン酸のヤバい側面を見るための、その前段階としてなのですが。
酵素
酵素をダイエット目的だかなんだかで、サプリとして摂取するのはマジで愚かだと思います。
Perfumeのライブをどうせ口パクだからとかいって見下すのと同じくらい愚かです。
酵素が何かというと、それは辞書を引くまでもなく「触媒」であって機能に基づいた分類です。
意味的には、「受容体」とか「抗体」とかいった言葉と同格だと思います。
触媒は促進する化学反応とセットで初めて意味を持ちますから、「酵素一般」を摂取するなんて行為は意味を成しません。
もちろん、経口で摂取することが全くの無益なわけではない「ある特定の」酵素も中にはあります。
が、大したものはありません。
もはや効き目が怪しくて保険適用から外されそうなリゾチーム、自己判断で使って良いOTCでの胃腸薬に含まれる消化酵素(大根のジアスターゼなど)くらいのものではないでしょうか。
- 参照資料:リゾチーム塩酸塩製剤「アクディーム®」「ノイチーム®」「レフトーゼ®」の
慢性副鼻腔炎に係る効能・効果削除の承認の見込みについて
新薬開発の話題で最近よく見るのは「抗体」ですが、「酵素」を作ろうとしているなんて話は滅多に聞きません。
現代の技術を持ってしても、酵素のデザインは難しいのです。
要するに、現状では胡散臭い会社しかこんなもんで商売しようなんて考えてないのです。
なので、胡散臭い商売がしたいのでなければ、酵素はサプリメントとして有用だなんて考えはとっとと捨てることです。
そんなことより遥かに面白いのが、いかにして酵素が「触媒」として機能しているか、という話です。
安定のエステルを平穏な暮らしのなかで壊す
ゆくゆくはカルバミン酸との関連で議論をしたい都合上、コリンエステラーゼという酵素について見てみます。
この酵素は、アセチルコリンを分解する反応を触媒します。
僕はアセチルコリンの加水分解を実験でやったことはありませんが、エステルの加水分解は酸か塩基を加えてpHを7.4よりかなりの程度上か下かに振った上で、さらに加熱して数時間かけてやっていたように記憶しています。
エステルは基本的には、生理的な条件で勝手に分解していくほど不安定ではありません。
戦争状態のような激しい環境に置かれないと壊れないのです。
ところが、そんなアセチルコリンのエステルが、平穏な日常の中で壊されてしまうことがあるのです。
そう、コリンエステラーゼがあれば。
基質特異性
普通反応の起こらない条件下でも反応を進行させる、というのは酵素の触媒としての凄さですが、酵素にはもう一つ強みがあります。
それが、基質特異性という性質です。
鍵と鍵穴に喩えられるように、酵素は特定の分子=基質だけを反応させます。
僕が実験室でやった条件(酸性あるいは塩基性+高温)では、エステルならなんでもかんでも加水分解されてしまうでしょうけど、このやり方を生体内でやっちゃうと大変なことになります。
生体内にはアセチルコリン以外にもエステルはいくらでもあって、例えば細胞膜の主成分リン脂質はエステルですから、エステル全部を対象にした分解反応を起こしてしまうと生体にとって不可欠な細胞膜に猛烈なダメージとなります。
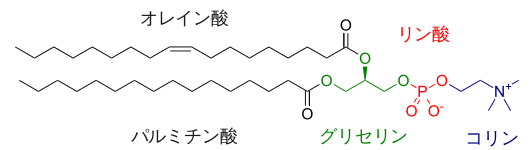 ↑これはWikipediaにあるリン脂質の一例ですが、グリセリンと脂肪酸、リン酸、さらにはリン酸とコリンをつなぐ結合は全てエステル結合であり、これらがことごとく分解されてしまえば細胞膜の構造も破壊されてしまうに違いありません。
↑これはWikipediaにあるリン脂質の一例ですが、グリセリンと脂肪酸、リン酸、さらにはリン酸とコリンをつなぐ結合は全てエステル結合であり、これらがことごとく分解されてしまえば細胞膜の構造も破壊されてしまうに違いありません。
が、コリンエステラーゼはアセチルコリンのエステルだけを、分解します。
細胞膜には一切傷など付きません。
どうしてそんなことが可能なのか?
それは、コリンエステラーゼが高度に設計されたマシンとして機能し、正確にアセチルコリンを捉える作りになっているからです。
もう、サプリなんて言わせない
酵素はこのように、生理的条件で起こりえない反応を起こしてしまう上に、しかも対象を限定できるという超ハイスペックの触媒なのです。
それも、せいぜい20種類に過ぎないアミノ酸だけで構成されている、タンパク質ごときでそんなことを成し遂げているのです。
多少サイズが大きくなってしまってはいますが、それにしてもすごいことです。
コリンエステラーゼがアセチルコリンを分解するサマを見れば、もう二度と、酵素をくだらないダイエットサプリの一種だなんてくだらない話題に留めることも無くなることでしょう。
その設計は最新の技術水準をも超越していて、酵素はまさに超兵器とでも言うべきものなのです。
アセチルコリンの掴まえ方
リボン構造だけでは分かりにくいので、分子の表面がどうなっているのかググるとこんな画像が出て来ました。
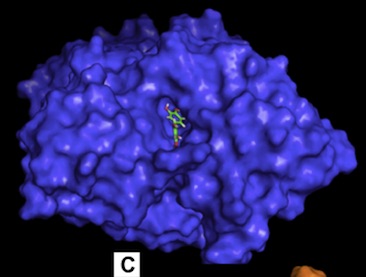
これはコリンエステラーゼ(青)に、基質(緑、但しここでは阻害剤)を作用させたときの図です。
- 参照元:ResearchGate
阻害剤が入り込んでいるポケット状の部位は、アセチルコリンが入り込んで分解されるのと同じ場所です。
こんな狭いところに都合良くアセチルコリンみたいなちっこい分子が迷い込むものか?という気がしてしまうものですが、そんな心配なんて不要なくらいにアセチルコリンはこのポケットにバンバン取り込まれて破壊されていくことでしょう。
コリンエステラーゼのポケットは、アセチルコリンを掴まえるための仕掛けが備わっているからです。
それは疎水性側鎖ゾーン、アスパラギン酸、及びチロシンであり、これらが絶妙な立体配置になっていることによります。
ポケットを簡略化した図を以下に示します。
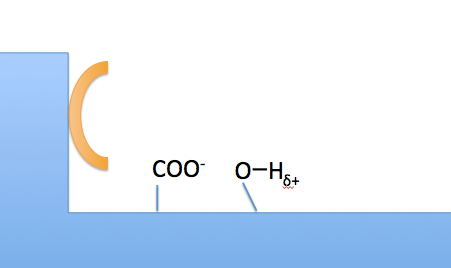 オレンジが疎水性側鎖ゾーン、カルボキシ基はアスパラギン酸側鎖、水酸基はチロシン側鎖を示しています。
オレンジが疎水性側鎖ゾーン、カルボキシ基はアスパラギン酸側鎖、水酸基はチロシン側鎖を示しています。
これらの構造はアセチルコリンをぴたりとトラップ出来るように配置されているので、こうなります。
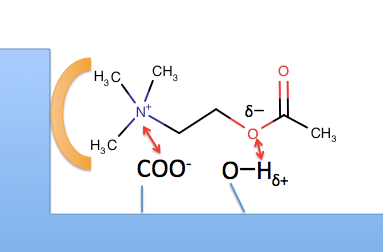
見事なまでの羽交い締めです。
色々な塩類が溶解しているために極性溶媒となっている体液中では、オレンジゾーンによる疎水性相互作用は強力に作用するでしょうし、イオン相互作用と水素結合という比較的強い分子間力をダブルで噛ますことで、アセチルコリンの自由に動けるはずの炭素鎖を完全に封じています。
もはやアセチル基に逃げ場はありません。
待ち構えているセリン、ヒスチジンの側鎖によって、いともたやすく、しかも超高速で分解されます。
忍び寄る影
さて、このように精密に仕立てられた装置・酵素ですが、これだけ周到に構成されたプロフェッショナルの構造を欺く輩がいます。
恐るべきその存在は、ある植物が生成します。
その名は、カラバル豆。
カラバル豆はコリンエステラーゼをものの見事に欺き、アセチルコリンでも無いくせにそのポケットにおさまり、挙げ句一時的ではあるものの動きを封じてしまいます。
そのときにカラバル豆が使うのが、そう、僕が一番簡単なアミノ酸として注目した、あのカルバミン酸なのです・・・!!!
カルバミン酸は生体内では、せいぜいオルニチン回路のカルバモイルリン酸、シトルリンに見られる程度の、あまり見かけることのない存在感でした。
それもそのはずです。
こいつ、生命にとっての生死を左右しうる、コリンエステラーゼを騙す能力を持っているのですから。
次回に続く。